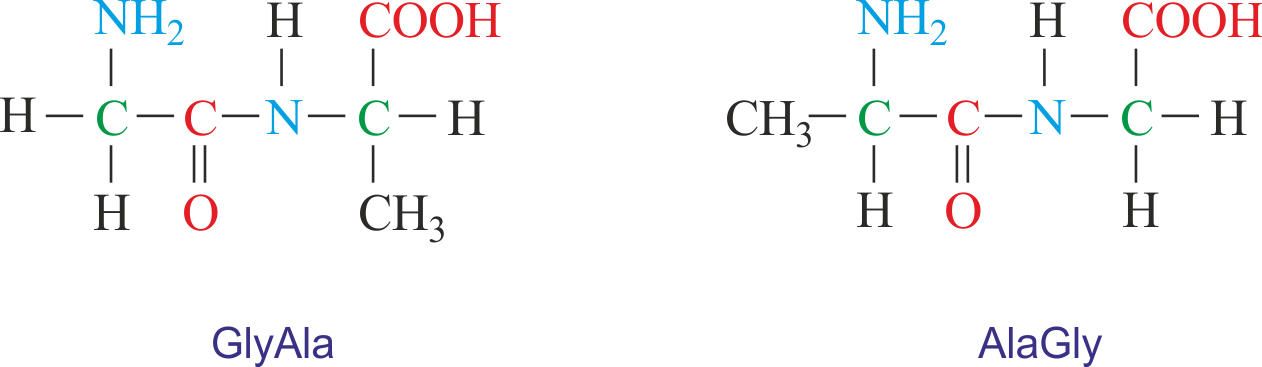Un dipeptide è un composto organico formato da due aminoacidi legati da un legame peptidico. Diversi dipeptidi sono fisiologicamente importanti e alcuni sono sia fisiologicamente che commercialmente significativi.
Struttura
Lineare
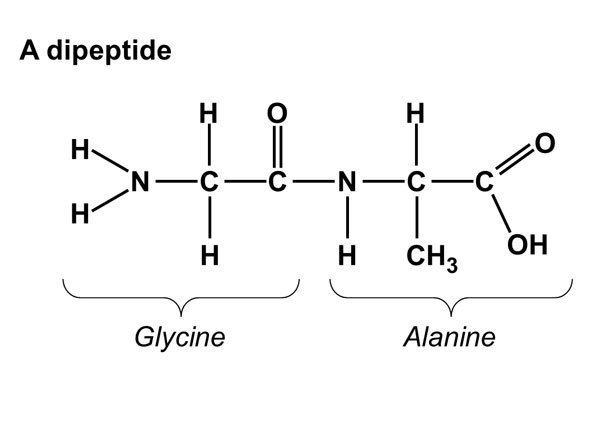
Come tutte le strutture proteiche, un dipeptide ha un'estremità da cui sporge il gruppo carbossilico chiamata estremità C-terminale, e un'altra estremità da cui sporge il gruppo amminico chiamata estremità N-terminale. Queste due porzioni sono quelle che generalmente reagiscono con le altre molecole.
A temperatura ambiente, i dipeptidi sono quasi tutti dei solidi bianchi, molto più solubili in acqua degli aminoacidi progenitori. Ad esempio, il dipeptide alanilglutammina ha una solubilità di 586 g/L, circa 10 volte la solubilità della glutammina che è 35 g/L. Poiché i dipeptidi sono inclini all'idrolisi, l'elevata solubilità viene sfruttata nell'alimentazione umana e non.
Ciclica
La ciclizzazione di un dipeptide porta alla formazione di dichetopiperazine. Spesso questa classe di molecole è formata da amminoacidi non proteinogenici.
Esempi rilevanti
Voci correlate
- Peptide
- Tripeptide
- Tetrapeptide
- Oligopeptide
- Polipeptide
- Proteina
- Legame peptidico
Altri progetti
- Wikimedia Commons contiene immagini o altri file su dipeptide